2. 江苏省常州环境监测中心,江苏省环境保护水环境生物监测重点实验室,江苏 常州 213001;
3. 常州大学环境与安全工程学院,江苏 常州 213164;
4. 江苏省南通环境监测中心,江苏 南通 226006
2. Key Laboratory of Environmental Protection of Water Environment Biological Monitoring of Jiangsu Province, Jiangsu Changzhou Environmental Monitoring Center, Changzhou, Jiangsu 213001, China;
3. School of Environmental and Safety Engineering, Changzhou University, Changzhou, Jiangsu 213164, China;
4. Nantong Environmental Monitoring Center of Jiangsu Province, Nantong, Jiangsu 226006, China
微塑料,学术界对其定义为直径<5 mm的塑料[1],其形状包括纤维、碎片和微珠等[2]。联合国环境规划署(UNEP)在2014年6月的首届联合国环境大会上发布报告指出,海洋里大量的塑料垃圾给海洋生态系统造成的经济损失每年高达130亿美元[3]。当前微塑料污染严重,其踪迹遍及全球海洋与淡水系统中[4]。而微塑料纤维是世界范围内海岸线、湖泊和河流中分布最广泛的微塑料之一[5-8]。有研究发现微塑料纤维对水蚤的毒性比微珠更大[9],会降低贻贝滤食藻类的速率[10],且易被吸入人体肺部,可能会引起疾病[11]。因此,有必要重点监测环境中的微塑料纤维污染。
迄今为止,水体中微塑料监测方法的研究已取得重要进展,但有关微塑料的分离技术仍处于起步阶段[12]。2015年,美国国家海洋和大气管理局(National Oceanic and Atmospheric Administration,NOAA)[13]提出一种基于玻璃漏斗的分离方法用于分离水体中的微塑料,但却忽视了微塑料纤维具有直接穿过孔径0.3 mm筛网的能力[14];此外,常用的容量瓶浮选[15]、直接浮选[16]等分离提取方法,均存在操作复杂、回收效率低等缺点。近年来,随着微塑料粒径的研究更加趋向于微纳级别,水体中残留的细颗粒泥沙等对微塑料的分离和观测造成的困扰也已成为当前亟待解决的问题[17-18]。
现建立一种简单高效的方法,适用于泥沙水样中微塑料纤维的分离和泥沙的去除。实验选择聚酰胺6(Polyamide 6,PA),丙烯腈-丁二烯-苯乙烯共聚物(Acrylonitrile butadiene styrene copolymers,ABS),聚丙烯(Polypropylene,PP)树脂制备微塑料纤维样品,以玻璃漏斗分离器[13]为容器,饱和氯化钠溶液(1.2 g/mL)为浮选介质,通过在静置阶段向内壁投加氯化钠颗粒(1 g/次)使内壁的泥沙沉降至漏斗颈中,打开止水夹排空泥沙,最后将水样抽滤至微孔滤膜(0.22 μm),以达到去除泥沙从而分离水样中微塑料纤维的目的。
1 材料与方法 1.1 仪器、材料与试剂仪器:玻璃漏斗(直径9 cm),EG37C电热板(LabTech公司),DM6801A表面温度计(胜利仪器公司),SGO-KK203视频显微镜(22寸显示器,深视光谷光学仪器有限公司),DHG-9140A电热恒温鼓风干燥箱(上海风棱实验设备有限公司),AL104电子天平(Mettler Toledo公司),HJ-6磁力加热搅拌器(金坛区西城新瑞仪器厂),SHZ-D(Ⅲ)型循环水式真空泵(邦西仪器科技有限公司)。材料:微孔滤膜(直径50 mm,孔径0.22 μm,上海兴亚净化材料厂);聚丙烯PA6 TP-4208聚酰胺(PA,集盛实业股份有限公司);ABS树脂PA-757(ABS,奇美实业股份有限公司);PP颗粒原料均聚T 03树脂(PP,中国石油化工集团有限公司)。
试剂:氯化钠、30%过氧化氢(均为分析纯,国药集团化学试剂有限公司);碘化钠(分析纯,麦克林试剂公司)。
1.2 实验方法 1.2.1 泥沙样品的制备采自自然河道中的底部沉积物,经过初筛分拣石块后,置于60 ℃烘箱中烘干至恒重,过1 mm标准筛[15, 19]以去除其他杂质。收集200 g筛下泥沙于1 L烧杯中,利用湿式过氧化氢催化氧化法(Wet Peroxide Oxidation,WPO)去除有机物[13]。依据密度差浮选原理[20],将干燥后的泥沙置于饱和氯化钠溶液(1.2 g/mL)中,磁力搅拌2 h,静置1 h,弃除上清液,重复以上操作3次,去除泥沙中的微塑料(密度<1.2 g/cm3)。为保证去除效果,再向干燥后的泥沙中加入800 mL饱和碘化钠溶液(1.8 g/mL),磁力搅拌2 h,静置1 h,弃除上清液。最后,加入800 mL超纯水,静置1 h,弃除上清液,重复以上碘化钠清洗步骤3次。铝箔轻覆,静置于烘箱中烘干至恒重后,混匀。获得不含微塑料(密度<1.2 g/cm3)的自然泥沙样品。以上操作在通风橱中进行,实验过程中均使用非塑料材质容器,所有敞口容器均用铝箔封盖,实验人员身着棉质服装,防止污染。
为更加接近自然水体中的泥沙含量,选择常州市某河道,随机选取9个点位,每个点位采集4.5 L水样,并设置3个平行。利用湿式过氧化氢催化氧化法消解去除有机物,在烧杯中用饱和氯化钠浮选去除微塑料,收集泥沙。参考《水质悬浮物的测定重量法》(GB 11901—1989)[21],称得泥沙质量最大为53.325 mg。
1.2.2 微塑料纤维的制备选择3种广泛使用的塑料原料PA、ABS、PP树脂作为样品制作对象。首先,分别取数粒树脂置于5 cm的玻璃培养皿内,80 ℃烘干2 h。随后,整体置于电热板上。设置低于熔融温度的初始温度,逐渐递增,缓慢升温。因电热板加热存在温差,实际融化温度由表面温度计测定修正,见表 1。
| 名称 | 密度/(g·cm-3) | 熔融温度/℃ | 实际融化温度/℃ |
| PA | 1.14 | 220~300 | 231.5 |
| ABS | 1.03~1.07 | 217~237 | 211.1 |
| PP | 0.90~0.92 | 164~170 | 188.3 |
达到设定温度后,利用2把不锈钢镊子分别夹取融化的微粒两端拉丝,收集入培养皿中。在视频显微镜下剪取长度为(1±0.25)mm,宽度为(200±30)μm的微塑料纤维,见图 1(a)(b)(c)。视频显微镜下放大180倍观察纤维表面,剪切处存在丝状或膜状边缘,但无可见气孔、裂缝等存在。用超纯水清洗,置于干净的玻璃培养皿中干燥保存,铝膜包裹,防止污染。

|
| 图 1 制备的PA、ABS、PP微塑料纤维(放大36倍) |
微塑料的密度作为重要的物理参数,决定了微塑料在水体中的分布和生物利用度[22]。因此,利用乙醇(0.8 g/mL),超纯水(1.0 g/mL),NaI(1.8 g/mL)配置密度梯度溶液20 mL[23],见表 2,测定微塑料纤维的表观密度。
| 体积比/(mL·mL-1) | 密度梯度溶液/(g·mL-1) | ||||
| 0.8 | 0.9 | 1.0 | 1.1 | 1.2 | |
| NaI/超纯水 | 0/20 | 3/17 | 5/15 | ||
| 乙醇/超纯水 | 20/0 | 8/12 | |||
截取PA、ABS、PP微塑料纤维段分别置于不同的密度梯度溶液中,于恒温培养箱25℃放置3 d后观察纤维在溶液中的漂浮状态,见图 2(a)(b)(c)(d)(e)(f)。表明制备的微塑料纤维样本的表观密度与实际密度相符。

|
| 图 2 微塑料纤维在密度梯度溶液中的漂浮状态 |
1.2.3 微塑料纤维的分离与泥沙的去除
预先将滤膜在103 ℃烘箱中烘干至恒重,记录每张滤膜的重量。分别挑选10根微塑料纤维于100 mL烧杯中,浸泡在饱和氯化钠溶液中,再与不同质量(0,0.01,0.05,0.25,1.25,6.25 g)的泥沙样本混匀,模拟浓缩后的泥沙水样。在漏斗中加入饱和氯化钠溶液(1.2 g/mL)至没过漏斗中部,倒入混合液,用少量饱和氯化钠溶液润洗,至液面于漏斗口下1.5 cm左右,铝箔轻覆。每组均设置3个平行。
水样静置1 h后向漏斗的内壁加入氯化钠颗粒(1 g/次)。打开止水夹,排去沉积于漏斗颈的泥沙;用饱和氯化钠溶液冲洗内壁,直至液面恢复至原始高度。重复以上步骤3~5次后,打开止水夹接取漏斗中剩余的水样,饱和氯化钠溶液冲洗内壁,将全部内容物转移入烧杯,真空抽滤,富集至微孔滤膜(0.22 μm),通过滤膜上的微塑料个数计算回收率(方法A)。不添加氯化钠颗粒的对照(方法B),除去氯化钠颗粒添加步骤,其余均与方法A相同;容量瓶浮选法(方法C)的步骤参照Nuelle等[15]的操作,浮选介质为饱和氯化钠溶液。
1.3 数据分析采用SPSS 23.0软件进行Pearson相关性分析,P<0.05为显著相关;采用Origin 2017软件绘制柱状图和散点图。
2 结果与讨论 2.1 不同材质与泥沙对微塑料回收的影响当选用PA微塑料纤维时,方法A和方法C的回收率均与泥沙质量相关性不显著(P>0.05);而方法B的回收率与泥沙质量相关性显著(P<0.05),总体上呈现每一质量组的平均回收率(96.67%~26.67%)随着泥沙质量的增加而减小,而1.25 g泥沙质量组平均回收率(46.67%)>0.25 g泥沙质量组(43.33%)。选用ABS和PP微塑料纤维时,3种方法对微塑料的平均回收率均与泥沙质量相关性不显著(P>0.05)。结果表明,泥沙质量对微塑料纤维的回收率影响较小。
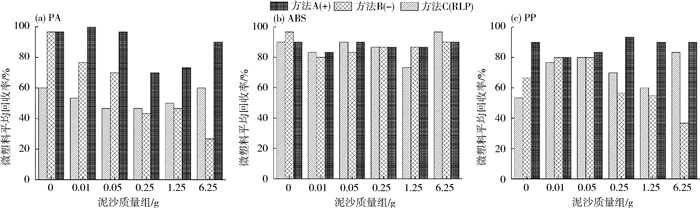
3种方法对不同泥沙质量组中PA,ABS,PP微塑料的平均回收率对比见图 3(a)(b)(c),“A(+)”,“B(-)”和“C(RLP)”分别表示静置阶段添加、不添加氯化钠颗粒和容量瓶浮选法。由图 3可知,3种不同材质微塑料的平均回收率呈现ABS>PP>PA。具有较高密度的ABS的平均回收率高于密度较低的PP,表明微塑料的密度对回收率影响较小。这与刘凯等[24]的实验结果一致,Buchan等[25]认为这是不同塑料表面自由能的差异导致了该情况。为尽可能模拟自然水样中的泥沙赋存,本实验未对泥沙的粒径进行分级,可能导致某一质量组混合的泥沙中粉砂[19]较多,吸附于纤维表面[26-27],重力增加,沉降到了漏斗底部,造成回收效率偏低。此外,不排除转移或抽滤过程中出现了损失,导致回收率降低。但对于3种不同材质的微塑料纤维,方法A的平均回收率较高,6组泥沙质量总平均回收率分别为PA(87.78%),PP(87.78%),ABS(87.78%)。同时也表明,微塑料纤维材质的不同未对方法A的回收率造成较大影响。
|
| 图 3 3种方法对不同泥沙质量组中PA、ABS、PP微塑料的平均回收率 |
2.2 不同方法对泥沙去除的影响
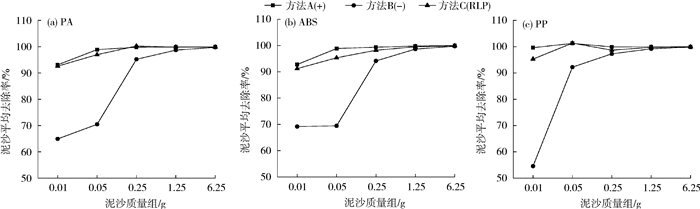
PA静置阶段添加氯化钠,ABS静置阶段不添加氯化钠颗粒和容量瓶浮选法对泥沙的去除率与泥沙质量相关性显著(P<0.05),而其他6组的泥沙去除率与泥沙质量相关性不显著(P>0.05)。3种方法对混合PA,ABS,PP微塑料纤维的泥沙平均去除率见图 4(a)(b)(c)。
|
| 图 4 3种方法对混合PA,ABS,PP微塑料纤维的泥沙平均去除率 |
整体上,方法A对泥沙的平均去除效果最优,其次是方法C,方法B的效果最差。3种方法对泥沙的平均去除效率随着泥沙质量的增加而上升,且呈现低泥沙质量时3种方法的差异大,而随着泥沙质量的增加平均去除率趋于一致。与运用方法A的PA、ABS、PP组相比,运用方法B的对照组对泥沙的总去除率分别降低了12.52%,11.54%,11.93%,方法C则分别减少了0.42%,1.15%,1.32%。这表明方法A中氯化钠颗粒的添加对去除率的提高作用明显。泥沙自然沉降后,仍有部分残留于漏斗的内壁。向内壁添加氯化钠颗粒,其沿壁面的下落运动,可以带动附着在内壁的泥沙沉降至漏斗底部,进一步去除了残留的泥沙。而方法C在倾倒的过程中水流的搅动易使已沉降底部的泥沙上翻,影响去除效果。由于相关研究较少,未能进行结果比较。
PA组0.25 g泥沙质量组的容量瓶浮选法,PP组0.05 g泥沙质量组的静置阶段添加氯化钠颗粒和容量瓶浮选法的泥沙平均去除率出现>100%的情况,分别为100.27%,101.25%和101.37%,这可能是夹取滤膜的过程中,滤膜边缘的缺损虚增了去除效率。但这并不影响去除效率的判定,比较抽滤后滤膜的颜色可以看出去除效果的显著差异。抽滤后的滤膜颜色对比见图 5,每组上层为不添加氯化钠颗粒,中层为容量瓶浮选法,下层为添加氯化钠颗粒。对比0.05和0.25 g泥沙质量组3种方法处理后的滤膜,可以明显看出膜上泥沙的减少,表明在方法A中静置阶段添加氯化钠颗粒对泥沙的去除有显著效果。

|
| 图 5 抽滤后的滤膜颜色对比 |
2.3 不同方法对微塑料回收的影响
总体上,方法A的平均回收率均要高于方法B和方法C。方法A对PA、PP、ABS的平均回收率分别比方法B高27.78%,25.28%,0.56%,比方法C高35%,17.22%,1.11%。3种方法对不同材质的微塑料纤维的平均回收率见表 3,呈现方法A>方法C>方法B。
| 材质 | 6组泥沙质量组总平均回收率 | ||
| 方法A(+) | 方法B(-) | 方法C(RLP) | |
| PA | 87.78 | 60.00 | 52.78 |
| ABS | 87.78 | 87.22 | 86.67 |
| PP | 87.78 | 62.50 | 70.56 |
| 平均回收率 | 87.78 | 69.91 | 70.00 |
同时,方法A对3种不同材质微塑料的平均回收率的相对标准偏差(RSD)为0,表明该方法具有稳定的浮选效果;该方法对PP的浮选效果(87.78%)与王元元等[19]得到的回收率(86.6%)基本相当,比刘凯等[24]得到的回收率(91%)略低;对PA的浮选效果(87.78%)比刘凯等[24]的90%略低。
3 结论通过在水样静置阶段向玻璃漏斗内壁添加氯化钠颗粒,显著提高了玻璃漏斗分离器对长度(1±0.25)mm,宽度(200±30)μm的PA,ABS,PP微塑料纤维的分离效率(87.78%)和泥沙去除效率(98.33%)。与不添加氯化钠颗粒和容量瓶浮选相比,PA,ABS,PP微塑料纤维的总平均回收效率分别提高了17.87%和17.78%,泥沙的总平均去除效率分别提高了12.52%和0.42%,可见,静置阶段添加氯化钠颗粒对微塑料纤维的回收和泥沙的去除均有显著效果。
致谢: 感谢常州大学陈智栋教授、单学凌博士对本研究提供的大力支持。
| [1] |
许霞, 侯青桐, 薛银刚, 等. 污水厂中微塑料的污染及迁移特征研究进展[J]. 中国环境科学, 2018, 38(11): 4393-4400. DOI:10.3969/j.issn.1000-6923.2018.11.050 |
| [2] |
DI M, WANG J. Microplastics in surface waters and sediments of the Three Gorges Reservoir, China[J]. Science of the Total Environment, 2018(616-617): 1620-1627. |
| [3] |
RAYNAUD J.Valuing plastic: the business case for measuring, managing and disclosing plastic use in the consumer goods industry[R].UNEP.Nairobi, Kenya: UNEP, 2014.
|
| [4] |
SU L, XUE Y, LI L, et al. Microplastics in Taihu lake, China[J]. Environmental Pollution, 2016, 216: 711-719. DOI:10.1016/j.envpol.2016.06.036 |
| [5] |
BROWNE M A, CRUMP P, NIVEN S J, et al. Accumulations of microplastic on shorelines worldwide: sources and sinks[J]. Computer Aided Optimum Design of Structures Ⅷ, 2011, 45(1989): 9175-9179. |
| [6] |
MCCORMICK A R, HOELLEIN T J, LONDON M G, et al. Microplastic in surface waters of urban rivers: concentration, sources, and associated bacterial assemblages[J]. Ecosphere, 2016, 7(11): e01556. |
| [7] |
MILLER R Z, WATTS A J R, WINSLOW B O, et al. Mountains to the sea: River study of plastic and non-plastic microfiber pollution in the northeast USA[J]. Marine Pollution Bulletin, 2017, 124(1): 245-251. DOI:10.1016/j.marpolbul.2017.07.028 |
| [8] |
WANG W, NDUNGU A W, LI Z, et al. Microplastics pollution in inland freshwaters of China: A case study in urban surface waters of Wuhan, China[J]. Science of the Total Environment, 2017(575): 1369-1374. |
| [9] |
ZIAJAHROMI S, KUMAR A, NEALE P A, et al. Impact of microplastic beads and fibers on water flea (Ceriodaphnia dubia) survival, growth and reproduction: Implications of single and mixture exposures[J]. Environmental Science & Technology, 2017, 51(22): 13397-13406. |
| [10] |
WOODS M N, STACK M E, FIELDS D M, et al. Microplastic fiber uptake, ingestion, and egestion rates in the blue mussel (Mytilus edulis)[J]. Marine Pollution Bulletin, 2018, 137: 638-645. DOI:10.1016/j.marpolbul.2018.10.061 |
| [11] |
PRATA, CORREIA J. Airborne microplastics: Consequences to human health[J]. Environmental Pollution, 2018, 234: 115-126. DOI:10.1016/j.envpol.2017.11.043 |
| [12] |
NGUYEN B, CLAVEAU-MALLET D, HERNANDEZ L M, et al. Separation and analysis of microplastics and nanoplastics in complex environmental samples[J]. Accounts of Chemical Research, 2019, 52(4): 858-66. DOI:10.1021/acs.accounts.8b00602 |
| [13] |
MASURA J, BAKER J, FOSTER G, et al. Laboratory methods for the analysis of microplastics in the marine environment: Recommendations for quantifying synthetic particles in waters and sediments[M]. NOAA Technical Memorandum NOS-OR & R-48, 2015: 1-39.
|
| [14] |
白濛雨, 赵世烨, 彭谷雨, 等. 城市污水处理过程中微塑料赋存特征[J]. 中国环境科学, 2018, 38(5): 1734-1743. DOI:10.3969/j.issn.1000-6923.2018.05.016 |
| [15] |
NUELLE M T, DEKIFF J H, REMY D, et al. A new analytical approach for monitoring microplastics in marine sediments[J]. Environmental Pollution, 2014, 184: 161-169. DOI:10.1016/j.envpol.2013.07.027 |
| [16] |
ZHANG S, YANG X, GERTSEN H, et al. A simple method for the extraction and identification of light density microplastics from soil[J]. Science of the Total Environment, 2018(616-617): 1056-1065. |
| [17] |
STOLTE A, FORSTER S, GERDTS G, et al. Microplastic concentrations in beach sediments along the German Baltic coast[J]. Marine Pollution Bulletin, 2015, 99(1-2): 216-229. DOI:10.1016/j.marpolbul.2015.07.022 |
| [18] |
GRACA B, SZEWC K, ZAKRZEWSKA D, et al. Sources and fate of microplastics in marine and beach sediments of the Southern Baltic Sea-a preliminary study[J]. Environmental Science and Pollution Research, 2017, 24(8): 7650-7661. DOI:10.1007/s11356-017-8419-5 |
| [19] |
王元元, 李先国, 张大海. 沉积物中微塑料的提取方法研究[J]. 世界科技研究与发展, 2016, 38(1): 105-109. |
| [20] |
THOMPSON R C, OLSEN Y, MITCHELL R P, et al. Lost at sea: Where is all the plastic[J]. Science, 2004, 304(5672): 838-838. DOI:10.1126/science.1094559 |
| [21] |
国家环境保护局.水质悬浮物的测定重量法: GB 11901—1989[S].北京: 中国环境科学出版社, 1989.
|
| [22] |
WANG J, TAN Z, PENG J, et al. The behaviors of microplastics in the marine environment[J]. Marine Environmental Research, 2016, 113: 7-17. DOI:10.1016/j.marenvres.2015.10.014 |
| [23] |
LI L, LI M, DENG H, et al. A straightforward method for measuring the range of apparent density of microplastics[J]. Science of The Total Environment, 2018, 639: 367-373. DOI:10.1016/j.scitotenv.2018.05.166 |
| [24] |
刘凯, 冯志华, 方涛, 等. 3种典型潮滩沉积物微塑料分离方法研究[J]. 水生态学杂志, 2017, 38(4): 36-42. |
| [25] |
BUCHAN R, YARAR B. Recovering plastics for recycling by mineral processing techniques[J]. JOM, 1995, 47(2): 52-55. DOI:10.1007/BF03221410 |
| [26] |
TEUTEN E L, SAQUING J M, KNAPPE D R U, et al. Transport and release of chemicals from plastics to the environment and to wildlife[J]. Philos Trans R Soc Lond B Biol Sci, 2009, 364(1526): 2027-2045. DOI:10.1098/rstb.2008.0284 |
| [27] |
TEUTEN E L, ROWLAND S J, GALLOWAY T S, et al. Potential for plastics to transport hydrophobic contaminants[J]. Environmental Science & Technology, 2007, 41(22): 7759-7764. |



